
Скачай приложение iTest
Готовься к школьным экзаменам в более удобном формате
Вариант 4
-
Характеристики твердого вещества.
-
Сульфид- анион образуется:
-
Для веществ с ионной кристаллической решёткой характерно:
-
В азотной кислоте между атомом азота и тремя атомами кислорода присутствуют связи:
-
Области применения алюминия и его сплавов.
-
Описание реакции хлора с железом.
-
Аммиак можно получить в лаборатории из веществ:
-
Ряд соединений, при диссоциации которых образуются катион металла и кислородсодержащий анион.
-
Способы устранения постоянной жесткости воды.
-
Цвет осадка раствора при добавлении щелочи к растворам хлорида меди(II), хлорида железа(II) и хлорида железа(III)
Вариант
Cu²⁺
Fe²⁺
Fe³⁺
A
голубой
бурый
зеленый
B
зеленый
голубой
бурый
C
бурый
зеленый
голубой
D
голубой
зеленый
бурый
-
Гетерогенная реакция.
-
Условие при котором химическое равновесие в реакции \(\text{2H}_{2(г)}+\text{O}_{2(г)}=2Н_2О_{(г)} \) смещается в сторону образования продукта:
-
Вещество, которому соответствует приведённое ионное уравнение гидролиза: \(\mathrm{SiO}_3^{2-} + \mathrm{H}_2\mathrm{O} =\mathrm{HSiO}_3^{-} + \mathrm{OH}^{-} \)
-
К макроэлементам, необходимым для развития растений относятся:
-
Утверждение, характеризующее ковалентную неполярную связь.
-
Кратность связи равна двум в соединениях:
-
Соединения, в которых присутствует атом в состоянии sp³ гибридизации.
-
Строка, в которой приведены свойства полиэтилена.
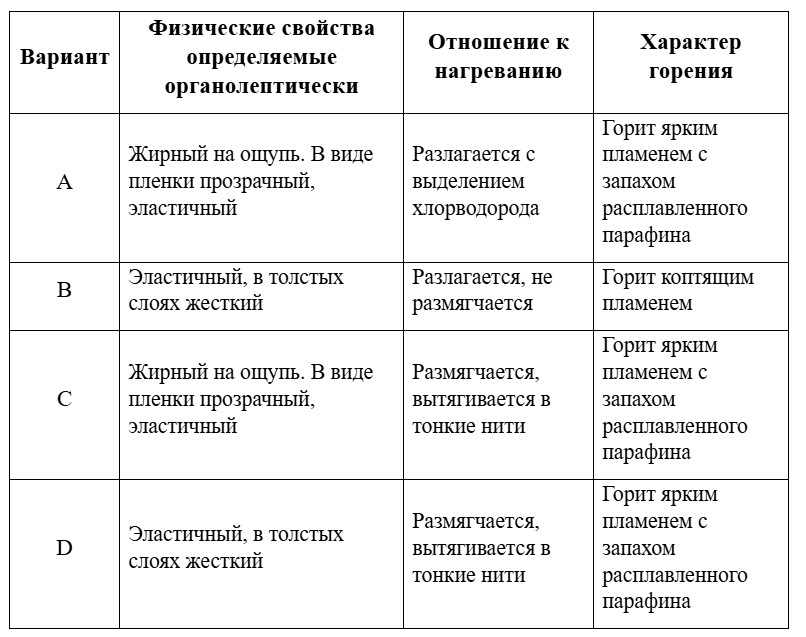
-
Формула углеводорода в составе которого 82,759% углерода и 17,241% водорода, относительная плотность по воздуху равна 2.
-
Объем газа, образующийся при разложении нитрата натрия массой 70,6г:
-
Объем хлора, необходимый для получения дихлорметана массой 127,5г из метана.
-
рН раствора объёмом 350мл, содержащий 0,0035моль гидроксида калия равна:
-
При повышении температуры с 10⁰С до 80⁰С скорость реакции увеличилась в 128 раз. Температурный коэффициент равен:
-
Сумма коэффициентов в уравнении реакции сульфита натрия с перманганатом калия в присутствии серной кислоты.
-
Дана цепочка превращений:
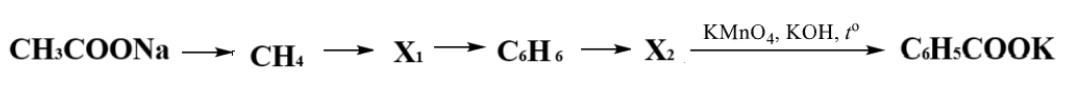
Веществами Х1 и Х2 являются:
-
Сопоставьте цвет пламени с катионом:
-
карминово-красное
-
кирпично-красное
-
Сопоставьте уравнение с типом химической реакции по числу и составу исходных и образующихся веществ:
-
реакция родонита калия с хлоридом железа (III)
-
реакция пропилена с бромной водой
-
Сопоставьте свойства соединений с типом кристаллической решётки.
-
высокая температура плавления, малая летучесть, большая твердость, электропроводность растворов и расплавов.
-
высокая тепло и электропроводность, ковкость и пластичность
-
Сопоставьте схему процесса с суммой коэффициентов в уравнении реакции.
-
K₂Cr₂O₇+NaNO₃ +H₂O
-
K₂Cr₂O₇+NaNO₃+H₂SO₄
-
Сопоставьте закон с автором, который сформулировал его:
-
«Номера аналогичных элементов отличаются на целое число семь или на кратное семи...»
-
«Свойства элементов, а также состав образуемых ими простых и сложных веществ находятся в периодической зависимости от их атомного веса»
-
Элементы, в которых распределение электронов на последнем уровне соответсвует формуле ns²p³
-
Пара веществ, реакция между которыми выражается ионным уравнением: Н⁺ + ОН⁻ = Н₂О
-
В 9% раствор уксусной кислоты массой 200г поместили соду.
Какова масса полученной соли и объем выделившегося газа, если выход продукта составил 80%.
-
Степень окисления марганца с каждом соединении: K₂MnO₄, Mn₃N₂, HMnO₄
-
При действии на смесь алюминия и магния массой 17.7г избытком соляной кислоты выделилось 19.04дм³ газа.
Массы алюминия и магния и массовая доля алюминия в смеси:





