
Скачай приложение iTest
Готовься к школьным экзаменам в более удобном формате
Вариант 3
-
Как изменяются окислительные свойства в периодической таблице?
-
Аммиак образуется в реакции:
-
Продуктами разложение нитрата никеля (II) являются:
-
Для определения альдегидов используют:
-
Укажите формулы основных оксидов.
-
К реакции межмолекулярного окисления относится:
-
Ионная связь – это связь, которая образуется:
-
Укажите ряд соединений, водные растворы которых проводят электрический ток.
-
Укажите последовательность процессов, происходящих при диссоциации ионных соединений.
-
Укажите математическое выражение скорости реакции для гетерогенной системы.
-
Что такое гомогенный катализ?
-
Увеличению выхода продукта в реакции N\(_2\) + O\(_2\) =2NO-Q способствует:
-
От чего не зависит внутренняя энергия тела?
-
На графике изображен термохимический процесс.
.png)
Укажите энергию активации.
-
Реакция при 40°С протекает за 32 сек, а при 10°С за 4 сек. Установите температурный коэффициент реакции.
-
Выражение константы равновесия для уравнения \(CuO_{тв}+H_{2(г)} = Cu_{тв}+H_2O_{(г)}:\)
-
В уравнении реакции А+В=2С, начальные конценртации А и В равны 1 моль/л каждая. Вычислите равновесные концентрации, если известно, что константа равновесия равна 25.
-
Укажите в какой реакции сера проявляет восстановительные свойства.
-
При сгорании 28,8 г вещества образовалось 44,8 л углекислого газа и 43,2 г воды. Плотность паров этого вещества по водороду равна 36. Молекулярная формула вещества:
-
25 г цинка поместили в раствор соляной кислоты массой 200 г с массовой долей кислоты 35%. Масса полученной соли и объем выделившегося газа равна:
-
Объем выделившегося газа на катоде при электролизе раствора бромида калия массой 124 г с массовой долей соли 25% составил:
-
Сколько оксида бария необходимо прореагировать с соляной кислотой для получения хлорида бария массой 30 г учитывая, что выход продукта составит 70%?
-
Укажите строку в которой верно указаны факторы, обеспечивающие характерные физические свойства металлам.
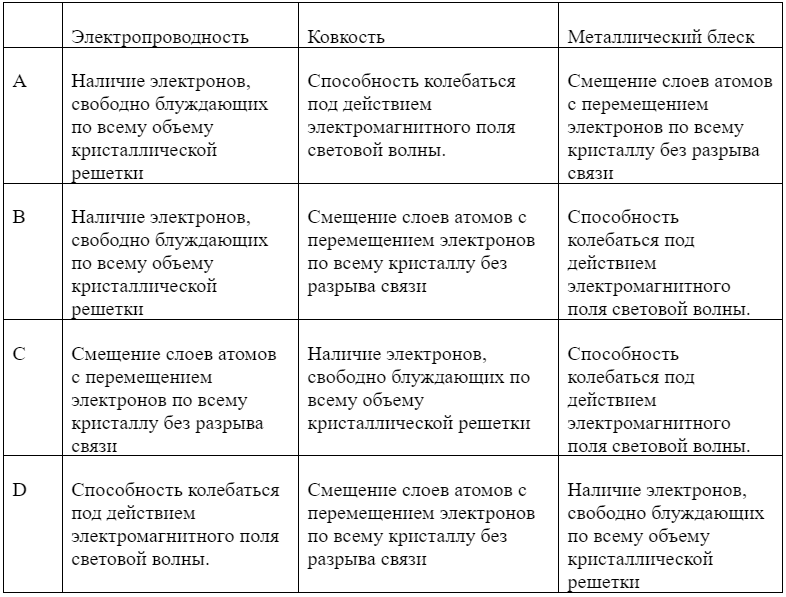
-
В раствор, содержащий 50 г нитрата серебра добавили 50 г хлорида калия. Масса образовавшегося осадка равна:
-
Структурная формула 2-хлор-3-метилбутановой кислоты:
-
В ионе аммония образуются связи:
-
Условия при которых возможна цис-транс изомерия:
-
Сколько хлора необходимо для получения 120 г хлорпропана, учитывая, что выход продукта реакции составляет 75%?
-
Смесь железа и оксида железа(III) прореагировали с раствором соляной кислоты массой 73 г с массовой долей кислоты 20%. При этом выделилось 1,12 л (н.у.) газа. Масса смеси, железа и оксида железа составляют:
-
Характеристика структуры алкенов:
-
Сопоставьте вид связи с формулами соединений:
-
ковалентная
-
ионная
-
Сопоставьте классы веществ с формулами соединений:
-
альдегид
-
кетон
-
Сопоставьте формулы солей с их названиями:
-
\(NaH_2PO_4\)
-
\(Mg(OH)Cl\)
-
Сопоставьте реактивы, вступающие в реакцию с массой соли, которая образуется, если в реакцию вступает 1 моль щелочи:
-
\(Al_2O_3+2NaOH\)
-
\(Al(OH)_3+NaOH\)
-
Сопоставьте глобальные проблемы, с причинами из возникновения:
-
разрушение озонового слоя
-
тепловой эффект





