
Скачай приложение iTest
Готовься к школьным экзаменам в более удобном формате
Вариант 2
-
Определение понятию «молекула» которое было сформулировано в 1960 г:
-
Укажите заряды элементарных частиц.
-
Укажите верное утверждение об изотопах.
-
3 электрона на р- подуровне имеют атомы элементов:
-
Что образуются при присоединении 2 электронов атомом серы?
-
К окислительно- восстановительной реакции относится:
-
Ковалентная связь – это связь, которая образуется:
-
Укажите ряд электролитов.
-
Укажите последовательность процессов, происходящих при диссоциации соединений с ковалентной связью.
-
Укажите математическое выражение скорости реакции для гомогенной системы.
-
Установите зависимость скорости реакции от температуры.
-
Укажите пару веществ реакция между которыми является необратимой.
-
Внутренней энергией называют:
-
Что такое энергия активации?
-
Температурный коэффициент реакции равен 3. Как изменится скорость реакции при повышении температуры с 10°С до 30°С.
-
Выражение константы равновесия для уравнения \(2CO+O_2=2CO_2\):
-
Вычислите константу равновесия реакции 2А+В=2С, если равновесные концентрации [A] = 0.04 моль/л, [B] = 0.03 моль/л, [C] = 0.06 моль/л.
-
Укажите в какой реакции сера является окислителем.
-
Осадок белого цвета образуется при добавлении к растворам солей сульфатов, хлоридов и карбонатов, соли с содержанием катиона:
-
Продуктами нейтрализации 1моль ортофосфорной кислоты 2 молями гидроксида натрия являются:
-
Свойства белого фосфора:
-
Вычислите объем водорода, который образуется при взаимодействии цинка массой 26г с соляной кислотой, если выход продукта составит 75%.
-
Укажите строку в которой верно приведены свойства галогенов.
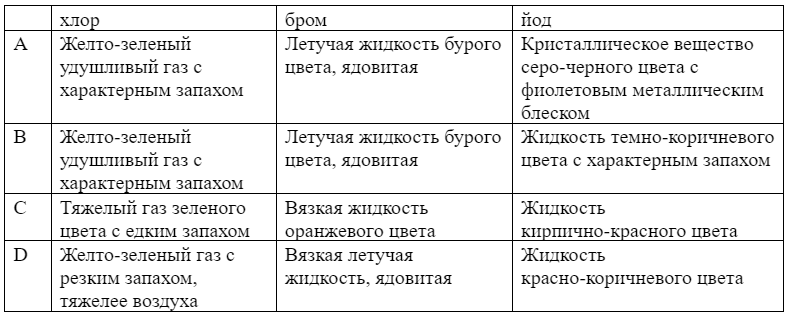
-
Оксид натрия массой 24.8 г прореагировали с раствором содержащим 21.9 г соляной кислоты. Масса образовавшейся соли равна:
-
Название соответствующее структурному строению: \(CH_3-CH_2-CH(CH_3)-CH(CH_3)-COH\)
-
Укажите области применения аммиака.
-
Для соединения с молекулярной формулой \(C_7H_{16}\) характерны виды изомерии:
-
Продуктами гидратации бутена-1 являются:
-
В ходе термической обработки образца природного известняка массой 30 г выделилось 5.6 л углекислого газа. Масса и процентное содержание карбоната кальция в данном образце составляют:
-
Функциональные группы аминокислот:
-
Сопоставьте название сплава с металлами, которые входят в его состав:
-
бронза
-
латунь
-
Сопоставьте описание способа получения металлов с его названием:
-
Получение металлов с помощью высокотемпературных реакций восстановления
-
Получение металлов из водных растворов их солей.
-
Сопоставьте фракцию нефти с его характеристиками:
-
лигроин
-
газойль
-
Сопоставьте реактивы, вступающие в реакцию с полученными продуктами:
-
\(Al_2O_3+2NaOH\)
-
\(Al(OH)_3+NaOH\)
-
Медь, массой 32 г реагирует с азотной кислотой различной концентрации с образованием соли меди и оксидов азота и воды. Сопоставьте реагенты с массой оксидов азота, которые образуются при их взаимодействии.
-
\(Cu+HNO_{3(разб)}\)
-
\(Cu+HNO_{3(конц)}\)





