
Скачай приложение iTest
Готовься к школьным экзаменам в более удобном формате
Вариант 5
-
Массовая и объемная доля кислорода в воздухе:
-
Электропроводностью обладают и растворы и расплавы веществ с кристаллической решеткой:
-
Описание процесса разрушения озонового слоя
-
Функции железа и кальция в организме
-
К микроэлементам относятся:
-
К реакции межмолекулярного окисления относится:
-
Определение металлической связи:
-
Укажите ряд соединений, водные растворы которых являются электролитами
-
Степень диссоциации показывает:
-
Укажи фактор не влияющий на скорость реакции.
-
Укажи строку в которой приводится гомогенный катализ.
-
В реакции CH₄(г)+2H₂O(г)=4H₂(г)+CO₂(г) -Q равновесие сместится вправо при:
-
Энтальпия реакции - это
-
На графике изображен термохимический процесс.
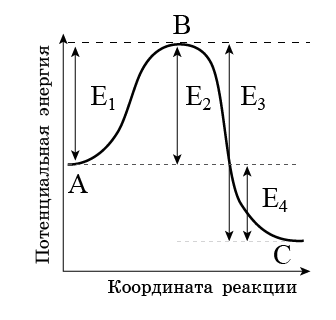
Укажи схему реакции, соответствующий процессу на графике.
-
Реакция при 20°С протекает за 16 сек, температурный коэффициент реакции равен 2. Определите время реакции при 50°С.
-
Формулы веществ, с которыми взаимодействует пентан
-
Вторичный спирт
-
44.8л пропана в присутствии света пропустили через бромную воду. В полученный продукт добавили спиртовый раствор гидроксида калия и нагрели. Масса органического продукта последовательных реакций.
-
Сумма коэффициентов продуктов реакции взаимодействия бромида натрия с перманганатом калия в нейтральной среде
-
Продуктами разложение нитрата никеля(II) являются:
-
Аммиак образуется в реакции:
-
Масса стали с содержанием углерода 0.8%, полученного из гематита массой 2т тонн, в котором примеси составляют 24%
-
Хром можно получить электролизом из сульфата хрома (III).В ходе реакции образуется еще 3 продукта.
Укажи строку в которой указаны все продукты полученные в ходе электролиза сульфата хрома массой 19.6г, их массы и объемы.
-
При сгорании кислородосодержащего органического соединения массой 35.2г выделилось 44.8л углекислого газа и 43.2г воды. (ρ=0.811г/см³) .
Формула соединения:
-
Масса металла, полученного из сульфида цинка массой 9.7 тонн, учитывая, что выход продукта на каждом этапе составляет 80%.
-
Сопоставьте катионы с описанием результатов качественной реакции для их идентификации
-
Cu²⁺
-
Ag⁺
-
Сопоставьте тип кристаллической решетки с формулами соединений с данной кристаллической решеткой:
-
ионная кристаллическая решетка
-
молекулярная кристаллическая решетка
-
Сопоставьте продукты электролиза водных растворов с формулами солей:
-
Сопоставьте формулу аминокислоты с его названием
-
CH₃-CH(NH₂)-COOH
-
CH₂ (NH₂)-(CH₂)-COOH
-
Сопоставьте описание значения переходного металла в живых организмах с его названием.
-
Оказывает влияние на кроветворение, минеральный обмен, рост, размножение и стабилизируют структуру нуклеиновых кислот.
-
Входит в состав ферментов, участвует в синтезе белков, участвует в фотосинтезе и дыхании растений.
-
Укажите схему реакций, протекающие с выделением осадка желтого цвета.
-
Укажите соединения для которых характерна реакция с кислотами.
-
Укажите верные утверждения о химическом равновесии.
-
Электрометаллургическим способом получают металлы:
-
Смесь массой 30г, состоящую из оксида магния и карбоната магния прокалили и получили 5.6л газа.
Массовая доля оксида магния и масса карбоната магния составляет:





